En el siguiente vídeo (2024) hablamos de las dosis recomendadas de suplementación de vitamina D. Causas y diagnóstico de deficiencia en vitamina D.
Definición de la vitamina D, ¿hormona o vitamina?
Ni una cosa ni otra, ambas. Si tenemos que decantarnos, hormona antes que vitamina (si queremos ser exactos, pro-hormona, pero con la idea de no enredar mucho, obvio explicar esto). Y esto es así debido a que la Vit D puede ser producida tras exposición de la piel al sol. Cuando entramos en contacto con radiación ultravioleta B, esta hormona viaja por el torrente sanguíneo hasta destino (órganos o células), teniendo impacto en mecanismos como: regulación del metabolismo del calcio a efectos en tejidos como la piel, ganglios linfáticos, páncreas, intestino o cerebro.
Una vez sintetizada la Vit D tras exposición solar, nos encontramos ante un producto inerte. Son varios los factores que influyen en la capacidad de síntesis por la piel, entre los que quiero destacar la cantidad de la melanina que tiene la persona. La melanina es un protector natural con el que contamos, al competir con 7-dehidrocolesterol y el color de la piel, edad, factores ambientales y hábitos de vida, tendrán influencia en la respuesta de la Vit D tras exposición solar.
Por ejemplo, en la siguiente gráfica, podemos ver el impacto que tiene la edad.
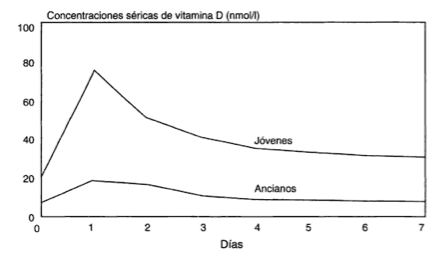 Holick MF et al. Age vitamin D, and solar ultraviolet radiation. Lancet 1989; 4: 1104:1105.
Holick MF et al. Age vitamin D, and solar ultraviolet radiation. Lancet 1989; 4: 1104:1105.
Un factor que puede explicar por qué se encuentra tan extendido el estado carencial de esta vitamina en la población sea la escasa exposición solar (de alguna forma se encuentra demonizado el acto de tomar el sol) o el uso extendido de protectores solares, necesarios para la prevención de patologías cutáneas pero que bloquean la síntesis de esta vitamina.
Y es que confiar en la vía exógena (alimentos) el aporte necesario es complicado, los números pueden no cuadrar. El motivo es el siguiente: algunos alimentos tienen buenas cantidades de vitamina D (pescados grasos, lácteos) pero no en forma de vitamina D2 o D3.
Los valores de referencia para determinar el estado fisiológico de la persona en relación a esta vitamina son: (como ng/ml de calcidiol en sangre)
- Por encima de 150 ng/ml es tóxica
- 30-60 ng/ml es óptima
- 20-29 ng/ml es suficiente
- 9-19 ng/ml es insuficiente (la carencia causa raquitismo, mayor riesgo de cáncer y fallos en las respuestas antimicrobianas)
El principal metabolito de la vitamina D es el calcitriol o 1,25(OH)2D, que se trata de una hormona esteroidea, implicada en mecanismos como homeostasis mineral, osteogénesis, respuesta inmune o diferenciación y crecimiento del tejido hematopoyético. Como hormona esteroidea que es, ejecuta sus acciones por acoplamiento (receptor nuclear-citosólico) que tras asociación con genes específicos produce incremento o descenso de su expresión.
En la conversión de 7-dehidrocolesterol a D3 participa como intermediario la previtamina D, que posteriormente se transforma en vitamina D (la temperatura corporal influye (ver gráfica apartado 2.1).
Calciferol = D2+D3. Vitamina D2 o ergocalciferol, aparece en las plantas y Vitamina D3 o colecalciferol en animales.
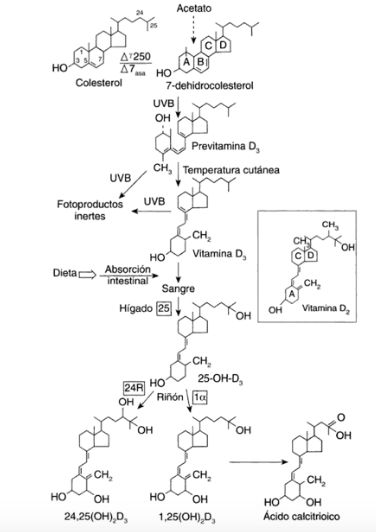
Ruta metabólica de la vit D.
2.1 Síntesis y metabolismo de la Vitamina D.
Holick MF, VitaminD. Primer on the metabolic bone diseases and disorders of chemical metabolism, MJ Fovus (ed), 1996.
Explicar el proceso es largo y complejo. Destaco los siguientes puntos.
a) La vitamina D sintetizada en la piel viaja hasta el hígado, donde es hidroxilada en el carbono 25, dando lugar a 25(OH)D (esta es la forma más abundante circulando). En este proceso destacamos la participación de la enzima D-25-hidroxilasa en mitocondrias y microsomas hepáticos.
b) La concentración media en sangre es de 30 ng/ml, de ahí que se utilice como valor de referencia en analíticas. Tiene una vida media de 15 días y el pool debe estar en equilibrio con las reservas de 25(OH)D, presentes en músculos y tejido adiposo.
c) Farmacología con metabolismo hepático puede transformar las hormonas esteroideas en productos biológicamente inactivos, por los que puede argumentar descensos en los valores de 25(OH)D tras ingesta de los mismos.
En relación a la síntesis, hay varios factores que participan en su regulación, destacando:
- Depósitos de vitamina D.
- PTH. Estados de hiperparatiroidismo se asocian a elevación en sangre de 1,25(OH)2D. También disminuye la síntesis renal de 24,25(OH)2D.
- Nivel de calcemia.
- Nivel de fosfatemia.
Tratado de nutrición. Manuel Hernández Rodríguez, Ana Sastre Gallego Ediciones Díaz de Santos, 1999.
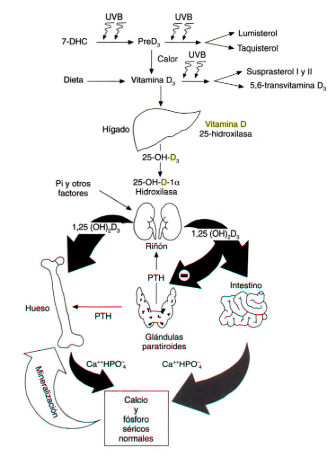
En la siguiente gráfica podemos ver las vías metabólicas que sigue la vitamina D.
Jordi Bover et al. Vitamina D, receptor de la vitamina D e importancia de su activación en el paciente con enfermedad renal crónica. Nefrologia 2015;35(1):28-41
De la gráfica anterior, destacamos en relación a la vitamina D y sus receptores:
- Intestino: aumenta la absorción de calcio y fósforo.
- Riñon: regula reabsorción de calcio y fósforo así como síntesis de calcitriol a través de PTH y FGF-23 (factor de crecimiento fibroblástico 23).
- Hueso: interviene en la regulación del recambio óseo.
- Paratiroides: inhibe la síntesis y secreción de PTH
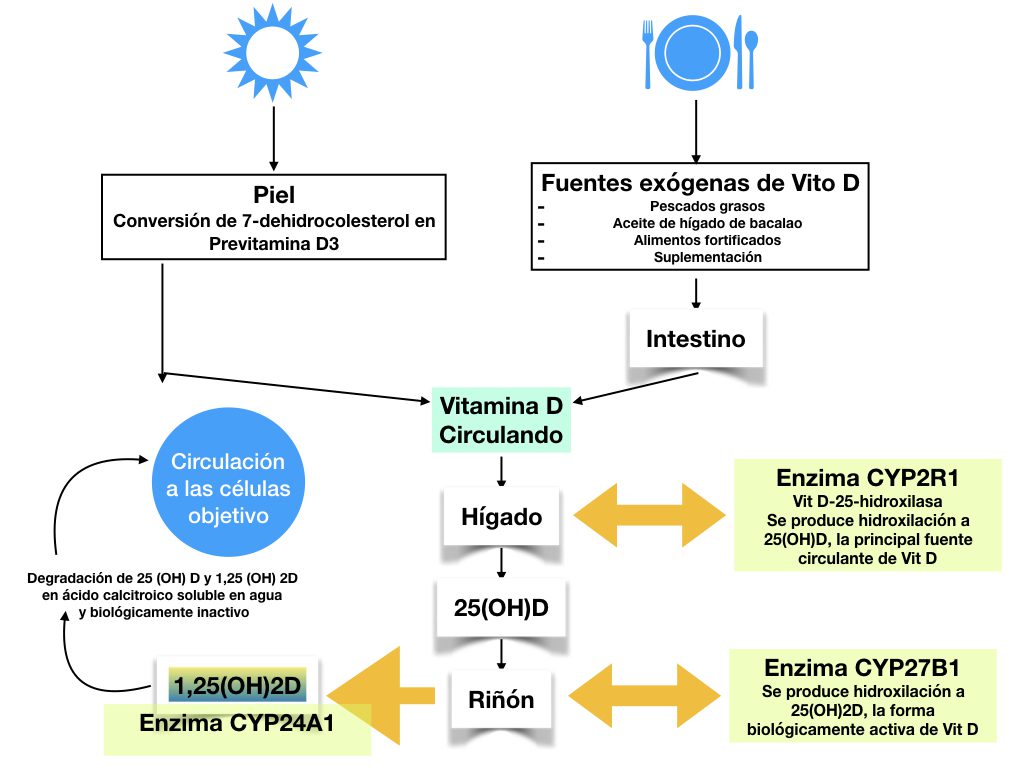
Resumen de la síntesis de vitamina D
Alrededor del 80% procede de radiación ultravioleta que induce a la conversión en la piel de 7-dehidrocolesterol a previtamina D3, alrededor del 20% procederá del aporte exógeno. Ya sea procedente del contacto con el sol, alimentos o suplementos, D2 y D3 son biológicamente inactivos y tanto en el hígado como riñón, se llevarán a cabo dos estados de hidroxilación, convirtiendo ahora sí, en la forma biológicamente activa de vitamina D, que se denomina 1,25(OH)2D. Tanto la vitamina D como sus metabolitos son transportados por proteínas de unión de la vitamina D (vitamin D binding protein, VDBP) y la entrada en la célula dependerá de esta asociación.
Acciones de la vitamina D
3.1 Esqueléticas
a) Protección esqueleto-mineral. Participa en el desarrollo y mantenimiento del esqueleto mineral, mediante la correcta formación osteoblástica y resorción osteoclástica.
b) Prevención y tratamiento del hiperparatiroidismo secundario y enfermedad ósea de alta recambio.
c) Activación de osteoclastos: maduración y activacón de osteoclastos mediada por los osteoblastos.
d) Apertura de los canales de calcio: incrementa sus niveles intramusculares favoreciendo la movilidad y cambios conformacionales, necesarios para una correcta función osteoblástica.
3.2 Extraesqueléticas
3.2.1 Protección renal
- Efectos antiproteinúricos.
- Aumento de la expresión de nefrina.
- Inactivación de NFkB (acción antiinflamatoria).
- Inhibición de TACE (tumor necrosis converting enzyme).
3.2.2 Protección cardiovascular
- Inhibición SRAA (sistema renina angiotensina aldosterona).
- Regulación ANP (atrial natriuretic peptide).
- Inhibición proliferación células musculares lisas.
- Disminución de la ateroesclerosis y calcificación vascular.
3.3.3 Control de la inflamación sistémica
- Inhibición linfocitos Th1.
- Activación linfocitos Th2.
- Inducción de CD4+CD25+
- Inhibición de mediadores TNFalfa, ICAM1 y VCAM1
3.3.4 Regulación de apoptosis
- Modulación de la expresión genética.
- Aumento de calcio intracelular.
- Apoptosis de células cancerígenas.
Vitamina D en activación inmune e inflamación.
Se ha visto que personas con bajos niveles de vitamina D presentan elevadas concentraciones de citoquinas proinflamatorias (TNFalfa, IL-6) así como proteína C-reactiva (estudio), de hecho, suplementar con vitamina D provoca un descenso en los niveles de estos marcadores (estudio). Aunque los niveles de Vit D van descendiendo con la edad, factores como baja exposición solar, dieta pobre en esta vitamina, farmacología, enfermedad crónica e incremento de masa grasa, contribuyen a empeorar su status en nuestro sistema.
Un aspecto que llama la atención es observar como en personas con edades tempranas, bajos niveles de vitamina D coexiste con un estado proinflamatorio subclínico, caracterizado por un progresivo incremento de los marcadores citados. Proteína C-reactiva, IL-6 y TNFalfa elevados junto con bajo nivel de vit D se asocia a: i) incremento de riesgo cardiovascular, ii) trastorno en el metabolismo de la glucosa, iii) enfermedad neurodegenerativa y iv) mortalidad general (estudio).
La vit D está presente en muchos tejidos en forma de receptores que intervienen en el proceso inflamatorio, jugando un rol destacado 1,25(OH)2D3 y 25(OH)D3, metabolitos que inhiben la producción de Il-6 y TNF-alfa (estudio), y aumentando la secreción de la citocina antiinflamatoria IL-10. La vit D (según estudios in vitro e in vivo) desplaza la respuesta inmune de una célula TH-1 (T-helper 1) a un TH-2 (antiinflamatorio).
Estas células forman parte de nuestro sistema inmunológico adaptativo, generados por linfocitos T y B (tras encuentro con antígeno se multiplican y producen citocinas e inmunoglobulinas). Los linfocitos T actúan sobre una importante variedad de células: células T, células B, células tisulares, macrófagos y células hematopoyéticas.
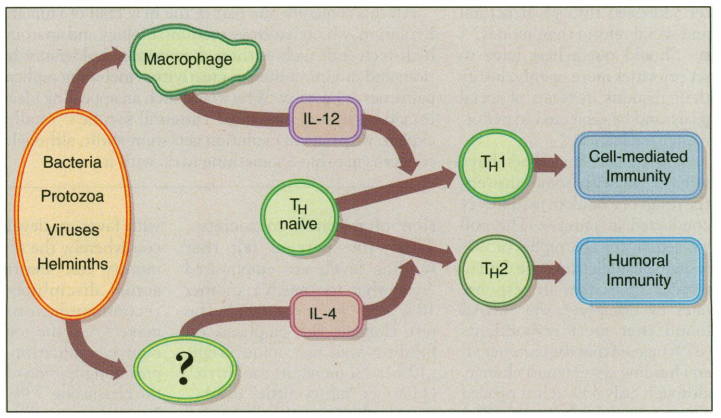
Dentro de las células T existen dos subgrupos de linfocitos, T helper 1 y T helper 2, dependiendo del tipo de citocinas que producen. Th 1 produce IL-2 e interferón γ (IFN-γ), encargados de estimular la inmunidad mediada por las células. Por su parte, TH2 segrega IL-4, IL-5 e IL-10, y favorecen la inmunidad humoral además de producir anticuerpos. Se da un proceso inhibitorio entre ambos grupos, IFN-γ inhibe la producción de TH-2 e IL-4 e IL-10 hacen lo mismo respecto a TH-1.
Que la respuesta inmune se decante a favor de la producción de TH-1 o TH-2 no es está del todo claro, pero la hipótesis que cobra más fuerza implica a determinadas citocinas, entre las que se destaca IL-12 y TNF-α, encargados de estimular la secreción de TH-1, mientras que IL-4 promueve la aparición del fenotipo TH-2. (estudio, estudio).
Scott P. IL-12: initiation cytokine for cell-mediated immunity. Science 1993;260:496-7.
De los 4 aspectos mencionados al inicio de este punto, el segundo hace mención a la relación entre bajos niveles de vitamina D y el trastorno en el metabolismo de la glucosa.
Suplementar con vitamina D reduce la proteína C reactiva circulante, como ya hemos citado. Parece existir una relación cruzada entre la vía de señalización inflamatoria y la vía de señalización posterior del receptor de insulina (estudio). El bajo nivel de respuesta inflamatoria crónica inducida por la vía del factor nuclear Kappa B y la interferencia del inhibidor de la cinasa de la vía de señalización de la insulina son una importante patogénesis de la Diabetes Mellitus 2.
(Si quieres ampliar conocimientos en relación a la regulación del factor nuclear Kappa B o NF-kB, te recomiendo este enlace)
Causas de deficiencia de vitamina D o deterioro funcional
(i) Disminución de la exposición a la luz solar
(ii) Fotosíntesis deteriorada en la piel
(iii) Dieta inadecuada
(iv) Absorción intestinal deteriorada
(v) Alteración de la conversión de vitamina D en metabolitos activos debido a enfermedad hepática o renal
(vi) Resistencia a los efectos biológicos de 1,25 (OH) 2D
(vii) Inactivación acelerada de los metabolitos de la vitamina D (barbitúricos, fenitoína y rifampicina)
(viii) Medicamentos (anticonvulsivos, glucocorticoides sistémicos, ketoconazol o antirretrovirales)
Relación entre niveles de vitamina D y cáncer
Existe correlación estadística entre déficit de vitamina D e incremento del riesgo de padecer cáncer.
Estudios in vivo e in vitro muestran que 1,25(OH)2 D inhibe la proliferación celular, angiogénesis (formación de nuevos vasos sanguíneos a partir de los ya existentes. Mecanismo habitual en situaciones como desarrollo embrionario o crecimiento, también es un proceso clave en el crecimiento tumoral, imprescindible para la diseminación del tumor y metástasis), invasión y promueve diferenciación y apoptosis.
En células tumorales, 1,25(OH)2 D/VDR (receptor de Vit D) participa en 3 mecanismos claves (estudio, estudio):
- Activa los inhibidores de cinasa dependientes de ciclina.
- Inhibe factores de crecimiento mitogénicos (IGF-1 y EGF).
- Promueve la actividad de TGF-β, por lo tanto, inhibe la proliferación celular y el crecimiento del cáncer.
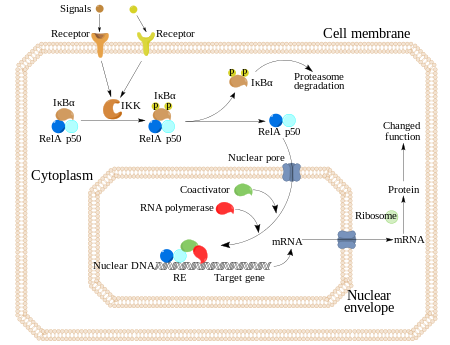
Factor de transcripción NF-kB
El factor de transcripción NF-kB regula la expresión de genes que controlan la proliferación celular, la apoptosis, la invasión y la metástasis (estudio). Se ha informado que 1,25 (OH) 2D / VDR puede suprimir las actividades de NF-kB, lo que da como resultado una disminución de la expresión de citocinas proinflamatorias y la inhibición de la proliferación celular y de la inflamación asociada al cáncer, con la desaceleración del crecimiento del mismo.
En la siguiente gráfica podemos ver el mecanismo de acción de NF-kB.
NF-kB juega un rol muy importante en la regulación de la respuesta inmune debida a la infección y su regulación defectuosa se relaciona con cáncer.
Como conclusión, está fuera de toda duda la importancia de vigilar el estatus de esta vitamina, algo que podemos hacer con una prueba analítica. Un estado carencial justificaría suplementación puntual (que debe pautar un profesional sanitario, por ejemlo, un dietista-nutricionista)
Hasta la próxima!